Ключевое различие между Хроматом и Дихроматом заключается в том, что Хромат имеет ярко-желтый цвет, а Дихромат — имеет ярко-оранжевый цвет.
Хромат и Дихромат представляют собой анионы, содержащие атомы хрома и кислорода. Следовательно, они оксианионы хрома. Часто используют эти термины в качестве общих терминов для обозначения соединений, содержащих эти анионы. Эти два аниона имеют близкие химические структуры, Хромат имеет один хромат-анион, тогда как Дихромат имеет два хромат-аниона в сочетании друг с другом. Но у них разный внешний вид.
Содержание
- Обзор и основные отличия
- Что такое Хромат
- Что такое Дихромат
- В чем разница между Хроматом и Дихроматом
- Заключение
Что такое Хромат?
Хромат представляет собой оксианион хрома, имеющий химическую формулу CrO42-. Термин хромат, как правило используется для обозначения соединений, содержащих этот анион, как одну группу, то есть соединения, содержащие анион хромата, называются хроматами. Обычно хроматы имеют ярко-желтый цвет.

Атом хрома в этом анионе находится в степени окисления +6. Он имеет свойства умеренно сильного окислителя. Молярная масса этого аниона составляет 115,99 г/моль.
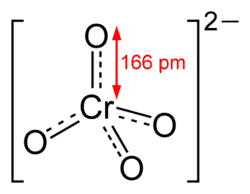
Хроматы вступают в реакцию с перекисью водорода, поскольку пероксидный анион замещает один или несколько атомов кислорода. В водном растворе, обычно, существует равновесие между хроматом и дихроматом. Тем не менее, можно обнаружить большое количество хромата при высоких значениях pH (выше 6,5 pH), где количество дихромата очень мало. Это означает, что в щелочных растворах преобладающим видом является хромат.
Что такое Дихромат?
Дихромат представляет собой оксианион хрома, имеющий химическую формулу Cr2O72-. Этот термин используют для обозначения соединений, содержащих Дихромат-анион, как одну группу. Например, дихромат калия, дихромат натрия являются дихроматами. Кроме того, соединения, содержащие дихромат в качестве аниона, имеют ярко-оранжевый цвет.

Молярная масса этого аниона составляет 215,99 г/моль. Дихромат имеет тетраэдрическую геометрическую структуру вокруг атома хрома.
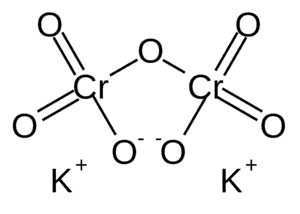
В водном растворе, обычно, существует равновесие между хроматом и дихроматом. Тем не менее, при низких значениях pH (ниже 6,5 pH) содержание дихромата больше при очень малом количество хромата.
В чем разница между Хроматом и Дихроматом?
Хромат и Дихромат представляют собой анионы, содержащие атомы хрома и кислорода. Следовательно, они являются оксианионами хрома. Ключевое различие между Хроматом и Дихроматом заключается в том, что Хромат имеет ярко-желтый цвет, а Дихромат имеет ярко-оранжевый цвет. Кроме того, ион Хромата имеет один атом хрома на анион, а ион Дихромата имеет два атома хрома на анион.
Еще, различие между хроматом и дихроматом заключается в их молярной массе. Молярная масса аниона Дихромата составляет 215,99 г/моль, тогда как молярная масса аниона Хромата составляет 115,99 г/моль. В водном растворе, обычно, существует равновесие между Хроматом и Дихроматом. Тем не менее, при высоких значениях pH (выше 6,5 pH) содержание Хромата намного больше, чем содержание Дихромата. Тогда как при низких значениях pH (ниже 6,5 pH) появляется больше ионов Дихромата.
Заключение — Хромат против Дихромата
Хромат и Дихромат представляют собой анионы, содержащие атомы хрома и кислорода. Следовательно, они являются оксианионами хрома. Ключевое различие между Хроматом и Дихроматом заключается в том, что Хромат имеет ярко-желтый цвет, а Дихромат имеет ярко-оранжевый цвет. В водном растворе, обычно, существует равновесие между Хроматом и Дихроматом. Тем не менее, при высоких значениях pH (выше 6,5 pH) содержание Хромата намного больше, чем содержание Дихромата, в то время как при низких значениях pH (ниже 6,5 pH) мы видим большее количество Дихромат-ионов.