Ключевое различие между Протием и Дейтерием состоит в том, что у Протия нет нейтронов в его атомном ядре, тогда как у Дейтерия есть один нейтрон.
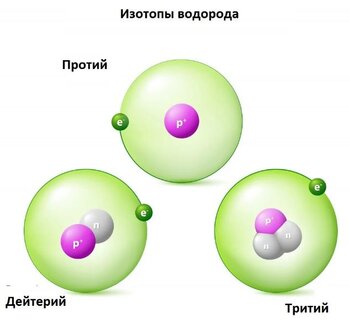
Протий и Дейтерий являются изотопами водорода. Они отличаются друг от друга по количеству нейтронов, присутствующих в их атомном ядре. Водород содержит один протон в атомном ядре: таким образом, атомный номер водорода равен 1. Существует три изотопа водорода и все три изотопа содержат один протон, а количество нейтронов у них разное. Называются они Протий, Дейтерий и Тритий, а обозначают их 1H, 2H и 3H. Значения в верхнем индексе являются атомными массами этих элементов.
Содержание
- Обзор и основные отличия
- Что такое Протий
- Что такое Дейтерий
- В чем разница между Протием и Дейтерием
- Заключение
Что такое Протий?
Протий — это изотоп водорода, который содержит один протон и один электрон. У него нет никаких нейтронов в атомном ядре. У него в ядре присутствует только один протон.
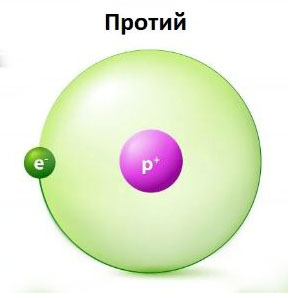
Этот изотоп назван так из-за присутствия этого единственного протона. Обозначается он как 1Н или водород-1, где 1 — атомная масса протия.
Протий является наиболее распространенным изотопом водорода. Количество его составляет около 99% всего водорода. Он является стабильным изотопом, так как протон в этом атоме никогда не подвергался распаду. Однако, согласно теориям, он подвергается распаду с очень большим периодом полураспада, из-за этого увидеть этот распад не представляется возможным.
Что такое Дейтерий?
Дейтерий — это изотоп водорода, имеющий протон, нейтрон и электрон. В отличие от протия, этот изотоп имеет протон и нейтрон вместе в атомном ядре. Следовательно, атомная масса этого изотопа равна 2. Дейтерий ещё называют водород-2 или 2Н. Он, также является стабильным изотопом водорода. Количество дейтерия очень мало по сравнению с протием и оно колеблется в пределах от 0,0026 до 0,0184%. В отличие от трития, дейтерий не является радиоактивным веществом и не является токсичным.

Вода обычно содержит водород-1 в сочетании с атомами кислорода. Но в ней может быть водород-2 в сочетании с кислородом, который образует воду. Эта вода называется — тяжелой водой. Химическая формула тяжелой воды — D2O, где D — это дейтерий, а O — кислород. Дейтерий и его соединения часто используются в химических экспериментах. Например, они применяются в качестве нерадиоактивных меток в экспериментах, таких как растворители, используемые в ЯМР-спектроскопии. Кроме того, тяжелую воду используют в качестве замедлителя нейтронов и теплоносителя для ядерных реакторов. Также, дейтерий является топливом для ядерного деления, и используют его в промышленности.
В чем разница между Протием и Дейтерием?
Существует три изотопа водорода: Протий, Дейтерий и Тритий. Ключевое различие между Протием и Дейтерием состоит в том, что у Протия нет нейтронов в его атомном ядре, тогда как у Дейтерия есть один нейтрон. Поэтому эти три изотопа отличаются друг от друга по количеству нейтронов, присутствующих в их атомном ядре. Кроме того, атомная масса протия равна 1, а атомная масса дейтерия равна 2.
Кроме того, изотоп водорода — Протий обозначается еще, как водород-1 или 1H, а дейтерий — как водород-2 или 2H. Протий является наиболее распространенным изотопом водорода, и его содержание составляет около 99% всего водорода. Тогда как Дейтерий сравнительно менее распространен (около 0,002%). Тем не менее, он также стабилен как Протий.
Заключение — Протий против Дейтерия
Существует три изотопа водорода: Протий, Дейтерий и Тритий. Эти три изотопа отличаются друг от друга в зависимости от атомной массы, которая является числом протонов и нейтронов в атомном ядре. Ключевое различие между Протием и Дейтерием заключается в том, что у Протия нет нейтронов в его атомном ядре, тогда как у Дейтерия есть один нейтрон.