
Что такое флуоресценция, фосфоресценция и люминесценция? Мы все ассоциируем их с эффектом свечения, но что отличает их друг от друга? Хотя все эти механизмы, с помощью которых светятся предметы, физически связаны и могут быть сгруппированы в рамках люминесценции, они фундаментально различаются по лежащему в основе физическому механизму, а также по эффектам.
Что такое Люминесценция
Люминесценция – простое объяснение
Существуют три основные формы люминесценции: флуоресценция, фосфоресценция и хемилюминесценция. Флуоресценция и фосфоресценция являются двумя формами фотолюминесценции. При фотолюминесценции свечение вещества вызывается светом, в отличие от хемилюминесценции, где свечение вызывается химической реакцией. И флуоресценция, и фосфоресценция основаны на способности вещества поглощать свет и излучать свет с большей длиной волны и, следовательно, с меньшей энергией. Основное отличие заключается во времени, которое требуется для этого. При флуоресценции излучение в основном мгновенное и поэтому обычно видимо только в том случае, если источник света постоянно включен (например, ультрафиолетовое излучение); в то время как фосфоресцентный материал может некоторое время накапливать поглощенную световую энергию и позже выделять свет, что приводит к послесвечению, которое сохраняется после выключения света. В зависимости от материала это послесвечение может длиться от нескольких секунд до нескольких часов.
Так что, если он сразу исчезает, это флуоресценция. Если он задерживается, это фосфоресценция. И если ему нужна активация, то это хемилюминесценция.
Представьте себе сцену в ночном клубе: зубы, глаза и ткань, светящиеся в черном свете, флуоресцентные, знак аварийного выхода фосфоресцентный, а светящиеся палочки хемилюминесцентные. Свет, излучаемый светящейся палочкой, является результатом двух химических веществ, которые смешались, когда маленькая капсула в палочке была сломана, и смешались при встряхивании палочки.
Люминесценция – комплексное объяснение
— Но как именно это работает? – спросите вы? Будьте готовы погрузиться в новые знания по физической химии. Чтобы понять принципы, лежащие в основе того, почему молекулы поглощают и излучают свет, нам нужно сначала взглянуть на электроны и понять их основное и возбужденное состояния и спин электрона, концепции, которые до сих пор не полностью поняты современной квантовой механикой.
Фотовозбуждение
Предпосылкой для фотолюминесценции, независимо от того, является ли она флуоресценцией или фосфоресценцией, является способность молекулы поглощать световое излучение, приводящее к электронному возбуждению. Связанный с молекулой электрон поглощает фотон и, следовательно, его энергию и становится возбужденным. Он переходит из основного состояния (Sо) в возбужденное состояние (Sп) мгновенно (~10-15 сек). Возбуждение может привести к тому, что электрон займет множество различных колебательных уровней (v=n) возбужденного состояния, в зависимости от точной длины волны поглощенного фотона. Возникающие в результате электронно-возбужденные состояния по своей природе нестабильны, и электроны будут релаксировать обратно в свое основное состояние с помощью нескольких комбинаций механических шагов, по-разному рассеивая энергию в процессе.
Вибрационная релаксация происходит чрезвычайно быстро (от 10–12 до 10–10 секунд) и приводит к диссипации энергии внутри одного возбужденного состояния за счет колебательной энергии, которая быстро рассеивается в виде тепла на соседние молекулы. Поскольку энергия не рассеивается при излучении света, колебательная релаксация представляет собой безызлучательный переход.
Внутренняя конверсия — еще один безызлучательный переход, изоэнергетический и к тому же быстрый (от 10-14 до 10-11 секунд). Он описывает переход одного электронно-возбужденного состояния (Sn+1) в колебательное состояние более низкого возбужденного состояния (Sn) того же энергетического уровня. При переходе энергия не рассеивается. Электрон может полностью рассеять первоначально поглощенную энергию только за счет колебательной релаксации и внутренней конверсии. В этом случае процесс релаксации будет полностью безызлучательным, молекула не будет ни флуоресцировать, ни фосфоресценировать, а вся поглощенная энергия будет рассеиваться за счет тепла. Вероятность возникновения радиационных событий по сравнению с полностью безызлучательной релаксацией определяет квантовый выход флуорофора и, следовательно, насколько ярко он будет светиться.
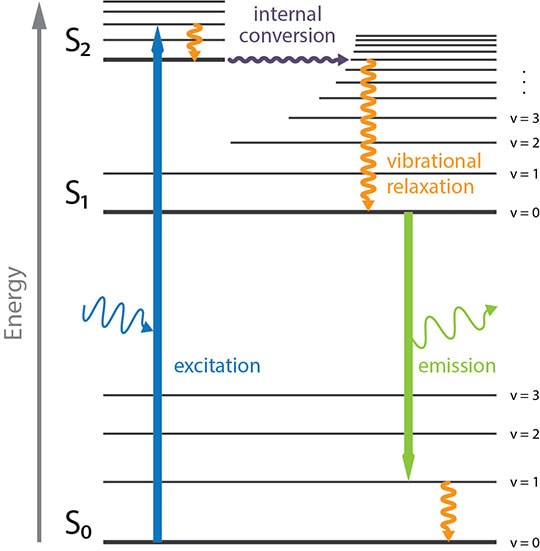
Примечание к рис.1. Электрон возбуждается, поглощая фотон с определенной длиной волны. Он релаксирует на бесколебательные уровни низшего возбужденного состояния (S1) через ряд безызлучательных переходов (колебательная релаксация и внутренняя конверсия). Дальнейшая релаксация в основное состояние (S0) за счет флуоресценции приводит к испусканию фотона с меньшей энергией и большей длиной волны, чем у возбуждающего фотона.
Что такое Флуоресценция
Одним из радиационных механизмов, посредством которого возбужденные электроны могут релаксировать, является светоизлучающий переход из низшего возбужденного состояния (S1) в основное состояние (S0) в результате быстрого (10-9 — 10-6 секунд) процесса, называемого флуоресценцией. Разница в энергии рассеивается путем испускания фотона. Из-за того, что электрон потерял часть первоначальной энергии возбуждения за счет колебательной релаксации, излучаемый фотон будет иметь меньшую энергию и, следовательно, большую длину волны.
Подобно возбуждению, излучение обычно может релаксировать на различные колебательные уровни (v=n) основного состояния (S0), что приводит к ширине полосы возможных длин волн испускаемого фотона. Электроны релаксируют с более высоких колебательных уровней (v=n) далее в бесколебательное состояние (v=0) за счет безызлучательной колебательной релаксации, если это необходимо. Результирующая излучаемая длина волны не зависит от длины волны возбуждения, поскольку обычно возбужденные молекулы распадаются на самый низкий колебательный уровень самого низкого возбужденного состояния в результате безызлучательных процессов до того, как произойдет испускание флуоресценции. В зависимости от молекулы безызлучательный распад может быть причиной рассеяния меньшей или большей части энергии возбуждения, что приводит к специфичным для молекулы сдвигам между длинами волн возбуждения и длинами волн излучаемого излучения. Это явление называется стоксовым сдвигом. Возможная длина волны фотона, который может быть поглощен при возбуждении, а также возможные длины волн излучаемого излучения, которые изменяются из-за распада флуоресценции на разные колебательные уровни, вместе определяют спектры возбуждения и излучения молекулы. Поскольку часто одни и те же электронные переходы участвуют в возбуждении и испускании флуоресцентной молекулы, спектры возбуждения и испускания часто напоминают отражения друг друга, что называется правилом зеркального отображения флуоресценции.
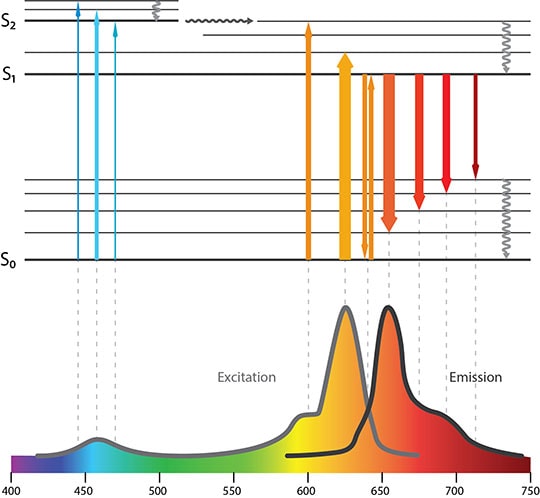
Примечание к рис.2. Вероятность возникновения событий возбуждения и испускания на разных длинах волн (обозначенная шириной стрелки) определяет спектры флуоресценции молекулы.
Что такое Фосфоресценция
Чтобы понять разницу между флуоресценцией и фосфоресценцией, нам нужно немного отвлечься от спина электрона. Спин — это фундаментальное неизменное свойство электрона и форма углового момента, определяющая поведение в электромагнитном поле. Спин электрона может иметь значение только ½, а ориентация спина может быть либо вверх, либо вниз. Поэтому спин электрона обозначается как +½ или -½, или, альтернативно, как ↑ или ↓. Два электрона на одной орбитали всегда будут иметь антипараллельный спин в основном синглетном состоянии (S0). При переводе одного электрона в возбужденное состояние электрон сохраняет свою спиновую ориентацию и синглетное возбужденное состояние (S1), где обе ориентации спинов остаются парными как антипараллельные. Все события релаксации при флуоресценции спин-нейтральны, и спиновая ориентация электрона сохраняется все время.
Однако это не так для фосфоресценции. Быстрый (от 10-11 до 10-6 сек) интеркомбинационный переход из синглетного возбужденного состояния (S1) в энергетически выгодное триплетное возбужденное состояние (T1) приводит к инверсии спина электрона. Триплетные возбужденные состояния характеризуются параллельным спином обоих электронов и являются метастабильными. Релаксация происходит через фосфоресценцию, что приводит к другому перевороту спина электрона и эмиттанса фотона. Возврат к релаксированному синглетному основному состоянию (S0) может происходить после значительной задержки (от 10-3 до >100 с). Кроме того, больше энергии рассеивается безызлучательными процессами во время фосфоресцентной релаксации, чем при флуоресценции, поэтому разница в энергии между поглощенным и излученным фотоном больше, а сдвиг длины волны более выражен. Таким образом, для фосфоресценции характерен больший стоксов сдвиг, чем для флуоресценции.

Примечание к рис.3. При интеркомбинационном переходе в возбужденное триплетное состояние (Т1) спин вовлеченного электрона переворачивается. Триплетные состояния метастабильны, а релаксация за счет фосфоресценции задерживается. Вероятность альтернативной релаксации безызлучательными событиями определяет квантовый выход как для флуоресценции, так и для фосфоресценции.
Что такое Хемилюминесценция
В то время как механизмы, участвующие в релаксации электронно-возбужденного состояния, в принципе такие же, как и при флуоресценции, хемилюминесценция заметно отличается в начальной генерации возбужденного состояния. В то время как большинство экзоэргических химических реакций высвобождают избыточную энергию реакции за счет тепла и являются экзотермическими, некоторые химические реакции могут привести к продукту в состоянии электронного возбуждения. Если возбужденное состояние релаксирует посредством люминесценции с испусканием фотона, этот процесс называется хемилюминесценцией. Если реакция катализируется биологическими ферментами, говорят о биолюминесценции, хотя механизмы идентичны.
Если энергия, генерирующая возбужденное состояние, возникает из-за механической энергии (например, при отрывании клейкой ленты), возникающее в результате излучение света называется триболюминесценцией.