Основное различие между Обратимым и Необратимым ингибированием фермента является то, что Обратимое ингибирование фермента инактивирует ферменты через нековалентное взаимодействие, тогда как Необратимое ингибирование фермента инактивирует ферменты посредством ковалентной инактивации активного центра. Кроме того, эффект ингибирования является обратимым при обратимом ингибировании фермента, но эффект ингибирования является необратимым при необратимом ингибировании фермента.
Обратимое и необратимое ингибирование фермента — это два метода механизма ингибирования фермента, ответственных за снижение активности фермента. Ингибиторы снижают совместимость субстрата и фермента, что приводит к ингибированию образования фермент-субстратных комплексов.
Содержание
- Обзор и основные отличия
- Что такое Обратимое ингибирование ферментов
- Что такое Необратимое ингибирование ферментов
- Сходство между Обратимым и Необратимым ингибированием ферментов
- В чем разница между Обратимым и Необратимым ингибированием ферментов
- Заключение
Что такое Обратимое ингибирование фермента
Обратимое ингибирование фермента представляет собой такой тип ингибирования фермента, при котором молекулы ингибитора связываются с ферментом посредством нековалентных взаимодействий. Здесь эти взаимодействия включают водородные связи, гидрофобные взаимодействия и ионные связи. Однако обратимые молекулы-ингибиторы не вступают в химические реакции с аминокислотными остатками активного центра фермента. Следовательно, обратимые ингибиторы могут быть удалены из фермента путем разбавления или диализа.
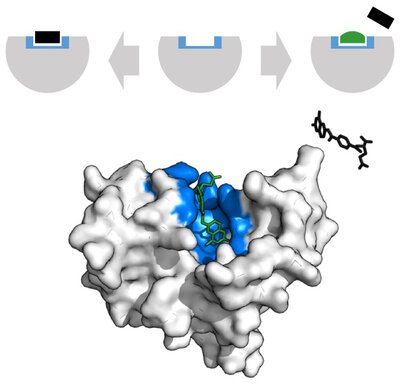
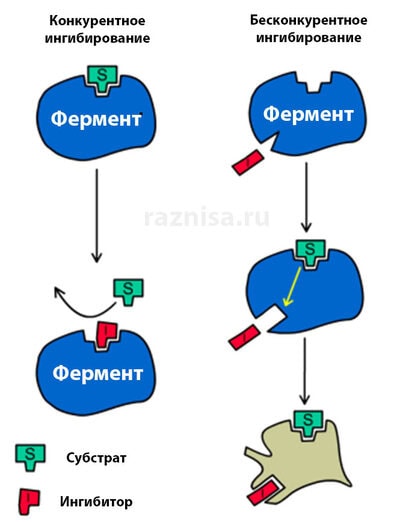
Существуют несколько типов обратимых ингибиторов ферментов, которые являются конкурентными, неконкурентными, бесконкурентными а также смешанными ингибиторами. Из них конкурентными ингибиторами являются соединения, имеющие структурное сходство с субстратом определенного фермента. Следовательно, он конкурирует с субстратом за достижение активного центра фермента, снижая ферментативное действие. Напротив, неконкурентные ингибиторы связываются с ферментом или комплексом фермент-субстрат в месте, отличном от активного центра. Тем не менее, это может изменить 3D-конформацию фермента, что, в свою очередь, снижает функцию фермента.
В свою очередь бесконкурентные ингибиторы связываются с комплексом фермент-субстрат, эффективно устраняя комплекс фермент-субстрат и, таким образом, уменьшая образование продукта. С другой стороны, смешанные ингибиторы могут связываться как с ферментом, так и с комплексом фермент-субстрат, высвобождая субстрат из образующего комплекса фермент-субстрат-ингибитор. В отличие от смешанных ингибиторов, неконкурентные ингибиторы не допускают диссоциации субстрата от образующегося комплекса фермент-субстрат-ингибитор.
Что такое Необратимое ингибирование фермента?
Необратимое ингибирование фермента является вторым типом ингибирования фермента с постоянными ингибирующими эффектами. Также основной существенной особенностью необратимых ингибиторов фермента является то, что они ковалентно связываются с аминокислотными остатками активного центра фермента. В связи с этим ингибиторы этого типа содержат реакционноспособные функциональные группы. К таким реакционноспособным функциональным группам относятся ионы тяжёлых металлов, азотистые иприты, альдегиды, галогеналканы, алкены, акцепторы Михаэля, фенилсульфонаты или фторфосфонаты. Примечательно, что эти реакционноспособные группы являются нуклеофильными и образуют ковалентные аддукты с боковыми аминокислотными цепями в активном центре.

Например, нервные газы, особенно DIFP, необратимо ингибируют биологические системы, образуя комплекс фермент-ингибитор. Обычно это происходит через определенную группу ОН серина в активных центрах определенных ферментов. Как правило, пептидазы, такие как трипсин и химотрипсин, содержат сериновые группы в активном центре, которые могут ингибироваться DIFP. Следовательно, этот тип ковалентных модификаций активного центра фермента может привести к постоянной инактивации фермента, и ферментативное действие трудно восстановить путем добавления избытка субстрата в среду.
Сходство между Обратимым и Необратимым ингибированием фермента
- Обратимое и необратимое ингибирование фермента представляют собой два типа механизмов ингибирования фермента;
- Они несут ответственность за снижение активности фермента;
- Они снижают совместимость фермента с его субстратом, ингибируя образование комплекса энзим-субстрат;
- Во время ингибирования молекулы ингибитора связываются с ферментом временно или постоянно;
- Естественным образом, ингибирование ферментов помогает регулировать обмен веществ. Также многие молекулы лекарств являются ингибиторами ферментов.
Разница между Обратимым и Необратимым ингибированием фермента
Обратимое ингибирование фермента относится к процессу связывания ингибиторов с ферментом посредством нековалентных взаимодействий, так что после удаления они позволяют восстановить функцию фермента. Между тем, необратимое взаимодействие фермента относится к процессу связывания ингибиторов с ферментом посредством ковалентных взаимодействий, так что их диссоциация занимает длительное время, навсегда устраняя действие фермента.
При обратимом ингибировании ферментов ингибиторы связываются посредством нековалентных взаимодействий, таких как водородные связи, гидрофобные взаимодействия и ионные связи. Напротив, при необратимом ингибировании ферментов ингибиторы связываются посредством ковалентных взаимодействий, которые модифицируют аминокислотные остатки с помощью реакционноспособных функциональных групп.
При обратимом ингибировании фермента комплекс фермент-ингибитор быстро диссоциирует, но комплекс фермент-ингибитор очень медленно диссоциирует при необратимом ингибировании фермента.
Обратимое ингибирование фермента может быть восстановлено, но необратимое ингибирование фермента занимает много времени для восстановления.
Типа обратимого ингибирования фермента — это конкурентное, неконкурентное, бесконкурентное и смешанное ингибирование, в то время как необратимое ингибирование фермента происходит посредством ковалентной инактивации активного центра фермента.
Некоторые из примеров обратимых ингибиторов ферментов включают DHFR, противовирусные препараты, такие как ритонавир, осельтамивир и типранавир. Между тем, некоторые примеры необратимых ингибиторов ферментов включают аспирин, дифторметилорнитин, инсектициды, такие как малатион, гербициды, такие как глифосат, и дезинфицирующие средства, такие как триклозан.
Заключение — Обратимое против Необратимого ингибирования ферментов
Обратимое ингибирование фермента — это процесс временного подавления действия фермента. Следовательно, при устранении ингибирующего действия функция фермента может быть восстановлена. Также обратимые ингибиторы связываются с ферментом посредством нековалентных взаимодействий. Следовательно, он позволяет быстро диссоциировать комплекс фермент-ингибитор, восстанавливая функцию фермента. Напротив, необратимое ингибирование фермента представляет собой процесс постоянного ингибирования функции фермента. Следовательно, диссоциация комплекса фермент-ингибитор является продолжительной. Кроме того, молекулы-ингибиторы ковалентно связываются с остатками активного центра фермента, блокируя образование комплекса фермент-субстрат. Основное различие между обратимым и необратимым ингибированием фермента заключается в механизме связывания ингибиторов с ферментом и вытекающих из этого эффектах.